630
2026-03-19

前言
在金藻纲(Chrysophyceae)中,既有仅需光能作为能量来源、以二氧化碳作为无机碳源进行生长的物种(自养生长),也有依赖有机碳源生长的物种(异养生长)。此外,已知部分物种能够同时利用无机碳源和有机碳源,这种营养策略被称为混合营养型。目前,人们对这些混合营养型生物会在何时利用何种代谢途径知之甚少,而这一选择可能取决于各自所处的环境条件。在利于不同营养行为的条件下开展生长实验,是理解混合营养型生长方式的必要基础。在此类实验中,总细胞计数为快速测定生长情况提供了一个可行指标。
在液体培养的生长实验中,尽管采用无菌操作,培养液仍存在较高的细菌污染风险,因为所需的培养基中含有有机碳源。对于藻类而言,无菌培养物指的是无细菌的培养物;与之相对,含有细菌的培养物则被称为带菌培养物。检测细菌污染的常用方法包括固体培养基涂布法、荧光显微镜检测法或光学显微镜检测法。这些方法不仅在建立过程中需要耗费精力,还需在总细胞计数之外额外操作。借助贝克曼库尔特生命科学公司生产的Multisizer 4e库尔特计数器不仅能快速且可靠地测定总细胞数,还能根据颗粒的大小分布检测出藻类培养物中是否存在细菌污染。
实验培养条件
混合营养型金藻奥杜藻(Ochromonas danica)与马尔汉棕鞭藻(Poterioochromonas malhamensis)于静置锥形瓶中培养,培养温度为20°C,光照强度为30 μmol光子·m⁻²·s⁻¹。奥杜藻(O. danica)与马尔汉棕鞭藻(P. malhamensis)的培养采用含可溶性有机碳源的培养基(见图1)。

图1:含有机碳源培养基中奥杜藻液体培养物的不同生长阶段
总细胞数测定
所有待测细胞悬液均使用Multisizer库尔特计数器测定培养物的总细胞数。实验选用100 μm小孔管,因预期藻类细胞大小在3-15 μm之间,对应的细胞体积约为20-1000 μm³(见图2)。取50-500 μl细胞悬液,加入12 ml Isoton II电解液中。每个样品需对细胞悬液与Isoton II电解液的混合液取500 μl进行三次重复测量,将三次测量的平均值保存为“#AV”格式文件。为消除培养基中纤维、晶体等杂质颗粒产生的背景噪音,每个样品需额外进行一次空白测量——即使用同等体积的培养基替代细胞悬液进行测定。通过Multisizer分析软件,将空白测量结果从平均值文件中扣除(以校正数据)。
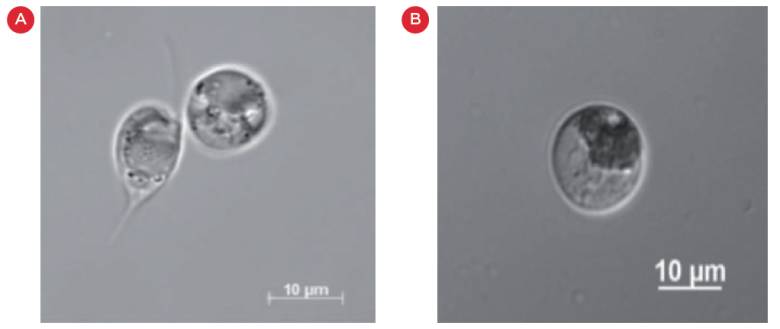
图2:不同藻类细胞的光学显微镜图像
(A)奥杜藻的两个单独细胞;(B)马尔汉棕鞭藻的单个细胞
藻类培养物的无菌性及Multisizer使用100 μm小孔管对细菌粒径范围颗粒的灵敏度
所有藻类培养物均通过Multisizer库尔特计数器检测是否存在细菌污染。
为研究Multisizer库尔特计数器使用100 μm小孔管时,对细菌特征粒径范围(<20 μm³)内颗粒的检测灵敏度,实验将马尔汉棕鞭藻培养物的等分样品,与不同浓度的热灭活细菌混合。添加的细菌浓度通过测定600 nm波长下的光密度(OD)确定:若测得OD600>1,则需稀释细胞悬液,直至可测得OD600<1。本实验所用细菌细胞悬液的初始计算密度为OD600=10。
藻类与细菌的混合悬液中,细菌细胞的光密度通过以下方式测定:制备一份对照悬液(用同等体积培养基替代藻类悬液),测定其光密度即可。通过Multisizer记录颗粒粒度分布;为作对比,同时对样品进行显微镜观察。为提高细菌的光学可检测性,将细胞悬液等分样品用核酸荧光染料(SYBR-Green)处理后,在荧光显微镜下(400倍放大)观察。
结果:两种藻类的粒径分布特征
奥杜藻与马尔汉棕鞭藻的细胞形态呈球形至水滴形,二者细胞大小相近(见图2)。通过Multisizer分析软件测得的这两种藻类的体积尺寸分布图也高度相似(见图3)。
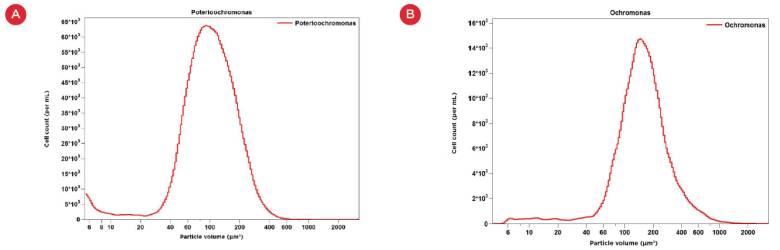
图3:所研究藻类物种的特征细胞体积分布
(A)马尔汉棕鞭藻;(B)奥杜藻
细菌污染的可检测性
马尔汉棕鞭藻与奥杜藻的培养物均为无菌培养物,即仅含藻类、不含细菌的培养物。在所有实验设置中,Multisizer搭配100 μm小孔管均可用于检测细菌是否存在。
在指数生长期,<20 μm³体积范围或约3 μm细胞直径范围内出现高浓度颗粒,是细菌污染的特征性表现,尤其当该范围内的颗粒密度超过藻类群体(20-2000 μm³体积或3.5-20 μm细胞直径)的颗粒密度时(见图4)。相应地,在未受污染的马尔汉棕鞭藻与奥杜藻培养物中,<20 μm³范围内未出现明显峰值(见图3)。
在生长曲线的指数生长后期与稳定期,细菌污染的检测仅能有限开展,因为裂解的藻类细胞也会在<20 μm³范围内形成峰值。将马尔汉棕鞭藻培养物与热灭活细菌悬液混合后,分别通过Multisizer 库尔特计数器和荧光染色法检测细菌:在细菌密度为OD600=0.05和OD600=0.03的样品中,显微镜下未观察到细菌;但通过Multisizer库尔特计数器测量时,在这些浓度下已能检测到细菌峰值(见图5)。当细菌密度为OD600=2时,无论是通过Multisizer库尔特计数器(图5A)还是显微镜(图5B),均能清晰检测到细菌。
因此,使用Multisizer库尔特计数器做藻类的总细胞计数时,可在实验过程中同时监测培养物是否存在细菌污染,且该方法的灵敏度与显微镜检测方法相当。
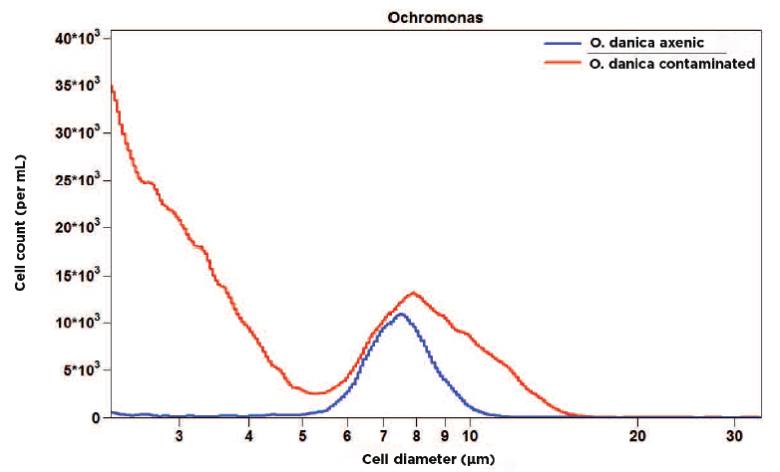
图4:指数生长期的奥杜藻培养物(含细菌污染:红色曲线;无细菌污染:蓝色曲线)在无菌培养物中(蓝色曲线),指数生长期仅能检测到藻类特征峰(5-20 μm);红色曲线则显示实验过程中细菌污染大量滋生的培养物的特征粒径分布,除藻类峰外,在直径<3 μm范围内可见典型的细菌峰。
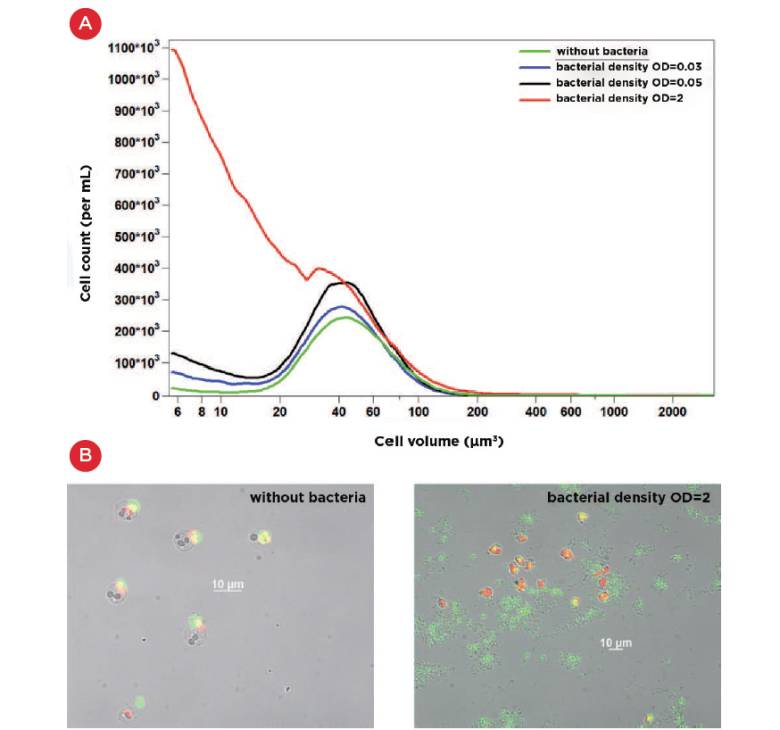
图5:添加与未添加热灭活细菌的马尔汉棕鞭藻培养物对比。(A)细胞体积分布:未添加细菌(绿色曲线)、细菌密度OD600=2(红色曲线)、细菌密度OD600=0.05(黑色曲线)、细菌密度OD600=0.03(蓝色曲线); (B)细菌的显微镜检测:核酸经SYBR-Green染色呈绿色,叶绿素自发荧光呈红色。未添加细菌的培养物中,绿色荧光可完全归属于特定藻类细胞;添加细菌的培养物中,藻类细胞外也出现绿色荧光,该荧光来源于同样被染色的添加细菌的核酸。
版权与免责声明:
① 凡本网注明"来源:中国粉体网"的所有作品,版权均属于中国粉体网,未经本网授权不得转载、摘编或利用其它方式使用。已获本网授权的作品,应在授权范围内使用,并注明"来源:中国粉体网"。违者本网将追究相关法律责任。
② 本网凡注明"来源:xxx(非本网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责,且不承担此类作品侵权行为的直接责任及连带责任。如其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。
③ 如涉及作品内容、版权等问题,请在作品发表之日起两周内与本网联系,否则视为放弃相关权利。