应用
应用
应用
背景:OA(Osteoarthritis,骨性关节炎)是一种慢性退行性关节疾病,其主要特征是关节软骨的进行性破坏,OA的发病机制受多种危险因素的影响,包括年龄、肥胖、性别、遗传易感性和创伤,晚期OA引起的关节功能障碍被认为是老年人残疾的主要原因,这给社会造成了巨大的经济负担。目前,临床治疗OA的药物还是以缓解疼痛症状为主,拮抗软骨退变的药物临床疗效并不确切,因此需要开发新的药物及其递送方式用于OA的临床治疗。 目的:(1)设计一种高效的褪黑素-壳聚糖微球载药体系;(2)建立人软骨细胞体外培养体系;(3)从体外细胞层面验证微球对人软骨细胞凋亡的拮抗作用。 方法:利用喷雾干燥法制作MT-CS,通过粒径分析仪、分光光度计、扫描电子显微镜对微球进行表征分析;提取进行全膝关节置换的OA患者膝关节软骨细胞培养,构建人软骨细胞OA模型,使用CCK-8法检测软骨细胞增殖情况;在构建的人软骨细胞OA模型上进行分组干预,通过酶联免疫吸附法(ELISA)检测软骨细胞上清液中肿瘤坏死因子-α、基质金属蛋白酶-13含量,Western Blot法检测软骨细胞中二型胶原的蛋白表达。 结果:利用喷雾干燥法制作的MT-CS具有较好的包封及载药率,在体外实验中,新构建的MT-CS较普通MT对人软骨细胞凋亡的拮抗作用明显增强。 结论:本实验设计优化了褪黑素壳聚糖微球的制作方法,并且在体外人软骨细胞OA模型中证实其具有较好的拮抗软骨细胞凋亡效果,为OA治疗的策略提供新思路。 ...
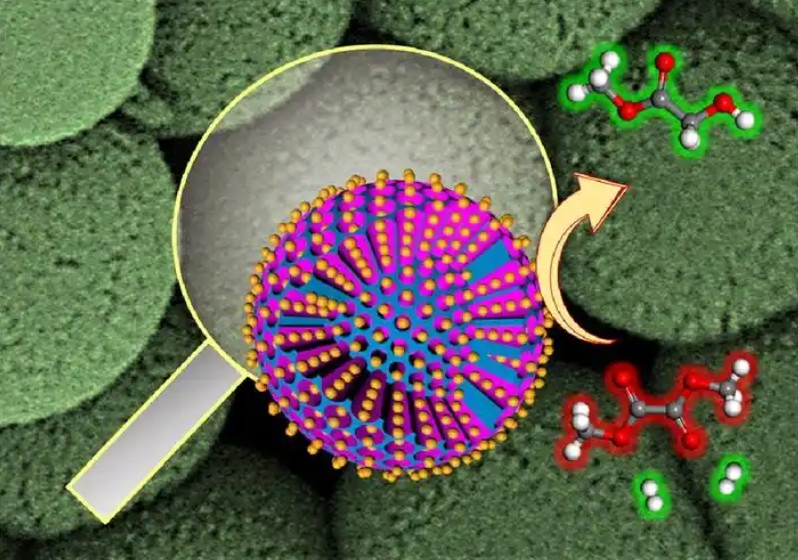
目的:基于微流控技术,选用PLGA(poly(lactic-co-glycolic acid),聚乳酸-羟基乙酸共聚物)高分子聚合物作为药物载体,负载GEF(Gefitinib,吉非替尼),构建GEF-PLGA载药微球,考察其载药效率、释放性质,并验证在肺癌细胞系和荷瘤小鼠上的抗肿瘤效果,为这种新型缓释载药微球的进一步临床转化提供科学依据。 方法:使用微流控技术制备GEF-PLGA载药微球,通过光镜、扫描电镜观察载药微球的形态、大小及粒径相关性。测量并研究GEF-PLGA载药微球的包封率载药率,测定体外缓释曲线,同时通过CCK8(Cell Counting Kit-8)实验及荧光染色法在PC-9肺癌细胞系上验证GEF-PLGA载药微球的抗肿瘤疗效。最后对荷瘤小鼠的肿瘤组织使用HE(Hematoxylin-eosin,苏木精-伊红)染色和免疫组化检测相关分子标志物,进一步验证抗肿瘤效果。 结果:我们成功制备了GEF-PLGA载药微球,通过光镜及电镜观察,其为表面带有小孔隙的圆形,粒径约为90μm,包封率约为95.16±1.35%;载药率约为19.17±0.20%;体外缓释曲线表明载药微球在体外可持续释放约15天,总释放药量65%左右。通过体外细胞抗肿瘤实验,发现GEF-PLGA载药微球生物相容性高,与微球共培养三天后PC-9细胞相对活力约30%,在荷瘤小鼠实验中,我们发现空白载药微球对肿瘤生长基本没有抑制作用,说明PLGA载药微球具有安全性,同时GEF-PLGA载药微球对于肿瘤的杀伤效果强于GEF裸药,HE染色和免疫组化定量结果进一步验证了载药微球抗肿瘤效果优于裸药。 结论:本研究通过微流控技术制备出了高包封率及高载药率的载药微球,GEF-PLGA载药微球在体内外实验中都显示出了良好的抗肿瘤效果,并在体内疗效评价中证实了相对于裸药的优越性。 ...
目的:以透明质酸(HA)为原料,在此基础上进行材料改性,通过微流控技术制备改性甲基丙烯酰化透明质酸(Hyaluronic acid Methacryloyl,HAMA)微球,利用化学键接枝负载白细胞介素-1受体拮抗剂(interleukin-1 receptor antagonist,IL-1 Ra)的BSA纳米粒(BSA nanoparticle,BNP),从而构建一种具有pH响应性能的水凝胶微球,研究其在治疗退变椎间盘中的作用。 方法:首先利用高碘酸钠与HA反应,获得醛基化透明质酸(Aldehyde-based hyaluronic acid,AHA)。随后加入甲基丙烯酸酐(methacrylic anhydride,MA)后,得到纯净的醛基化甲基丙烯酰化透明质酸(Aldehyde-based methacrylated hyaluronic acid,AHAMA)。通过微流控装置制备出单分散微球,与负载IL-1 Ra的纳米粒通过席夫碱化学键接枝,从而得到具有pH响应性能的改性HAMA微球(Modified MS)。通过光学显微镜、扫描电镜、能谱仪、傅立叶红外光谱、粒度仪、酶联免疫吸附试验等对微球进行表征测定。本研究体外实验中所使用的大鼠髓核细胞(Nucleus pulposus cells,NPCs)提取自大鼠尾椎椎间盘,通过活/死染色及CCK-8实验评价所制备材料的生物相容性。采用免疫荧光、Western Blot等方法评价在酸性条件下IL-1Ra的治疗作用。最后,对大鼠进行体内动物实验,通过X线、MRI等影像学技术,研究大鼠椎间盘高度和信号强度的改变。于手术后第4和第8周取出标本后,行H&E、番红固绿色染色及组织学染色,从组织学水平评价改性HAMA微球对椎间盘的修复修复。 结果:本研究采用微流控技术,获得了尺寸均一、可响应pH改变调整释放药物速率的改性HAMA微球。通过活/死染色与CCK-8实验,证实了改性HAMA微球的生物相容性良好,并可促进髓核细胞的增殖。通过免疫荧光、蛋白质印迹等方法,证实了改性HAMA微球具有抗炎、促进ECM修复的效果。动物实验中,影像学与组织学结果表明,Modified MS组显著优于其他实验组,术后4周、8周结果与NC组相比均无统计学差异,表明Modified MS组的椎间盘再生能力优异。 结论:成功制备联合IL-1 Ra的pH响应型改性HAMA微球,其能够缓慢释放IL-1 Ra,具有良好的生物相容性,在体外酸性环境下能持续抑制炎症反应,恢复细胞外基质。在体内促进退变大鼠椎间盘再生效果显著。因此,本课题组制备的联合IL-1 Ra的pH响应型改性HAMA微球为椎间盘炎症微环境下生物材料的再生应用提供了一种新的治疗策略。 ...
背景与目的: 颌面部烧伤、创伤和肿瘤常常带来颌面部皮肤的缺损,极大地影响患者的美观和生活质量。脂肪来源的间充质干细胞由于来源广泛、获取方便、具有多向分化能力和低免疫原性,因此在皮肤组织再生方面具有巨大潜力。与单层的间充质干细胞相比,三维间充质干细胞微球能更好发挥疗效,但是将间充质干细胞微球直接移植到体内仍然存在治疗效果不佳的问题,这可能与细胞微球受到外界不利刺激影响,迅速丧失三维结构有关。 为了解决这一问题,课题组前期将金属多酚网络(metal polyphenol network,MPN)材料包裹在牙周膜干细胞微球表面构建了牙周膜干细胞微球胶囊模型,系统的研究了MPN的抗氧化、抗菌和抗凋亡的特性,并证实MPN可以积极改善细胞微球的微生态环境,但课题组并未详细研究MPN材料对细胞微球自身抗炎性能的影响。本实验制备了脂肪来源的间充质干细胞微球(adipose derived stem cell spheroid,ADSC spheroid),将铁-单宁酸(ferrum-tannin,FeⅢ-TA)包裹在细胞微球表面构建脂肪干细胞微球胶囊(spheroid@[FeⅢ-TA]3),并进一步研究了 ADSC spheroid在MPN包裹下的三维状态和抗炎功能。 本课题主要包括以下研究内容:FeⅢ-TA涂层的表征及其对ADSC spheroid生物活性的影响;FeⅢ-TA涂层对 ADSC spheroid三维状态的影响;FeⅢ-TA涂层对ADSC spheroid体外抗炎功能和促进巨噬细胞向修复型巨噬细胞极化的影响及机制研究;利用小鼠皮肤缺损模型,验证spheroid@[FeⅢ-TA]3的增强的皮肤再生能力并研究其作用机制。 材料与方法: (1)Spheroid@[FeⅢ-TA]3的制备及生物活性检测。通过“单次自组装法”制备spheroid@[FeⅢ-TA]3胶囊;通过紫外-可见吸收光谱实验、扫描电子显微镜能量色散光谱实验和傅里叶变换红外光谱实验对FeⅢ-TA材料进行表征;通过细胞贴壁实验,研究FeⅢ-TA涂层的数量对 spheroid@[FeⅢ-TA]3贴壁的影响;构建了负载罗丹明B的spheroid@[FeⅢ-TA]3模型,通过共聚焦激光扫描显微镜(confocal laser scanning microscopy,CLSM)对FeⅢ-TA涂层进行观察;通过细胞计数试剂盒-8实验(cell counting kit-8,CCK-8),细胞流式凋亡实验体外检测ADSC的生物活性;最后通过小鼠皮下移植实验体内检测ADSC的生物活性。 (2)验证FeⅢ-TA涂层对ADSC spheroid三维状态和抗炎功能的影响及机制。将spheroid@[FeⅢ-TA]3播种在组织培养板上,通过相差显微镜和CLSM观察spheroid@[FeⅢ-TA]3的贴壁情况和三维状态;通过实时定量聚合酶链反应(Quantitative real-time polymerase chain reaction,qRT-PCR)检测细胞微球三维状态相关基因的表达;通过蛋白质微阵列和qRT-PCR,检测体外 spheroid@[FeⅢ-TA]3抗炎基因的表达和分泌,并用细胞培养上清液刺激巨噬细胞,检测spheroid@[FeⅢ-TA]3促进巨噬细胞向修复型巨噬细胞极化(Repair macrophage,M2 macrophage)的作用;最后通过RNA测序分析,研究FeⅢ-TA涂层对ADSC spheroid三维状态和抗炎功能影响的机制。 (3)验证 spheroid@[FeⅢ-TA]3对小鼠皮肤缺损愈合的作用及机制。将spheroid@[FeⅢ-TA]3植入到小鼠背部皮肤缺损处,观察其促进伤口愈合的效果;通过组织切片免疫荧光染色,观察spheroid@[FeⅢ-TA]3抗炎因子的分泌和促进小鼠巨噬细胞向M2型转化的作用。 结果: (1)构建了 ADSC spheroid胶囊,即spheroid@[FeⅢ-TA]3。紫外-可见吸收光谱实验、扫描电子显微镜能量色散光谱实验和傅里叶变换红外光谱实验表明FeⅢ-TA涂层在ADSC spheroid表面的成功包覆;CCK-8实验和细胞流式凋亡实验证明FeⅢ-TA涂层在体外对ADSC spheroid生物活性无显著影响(P>0.05);小鼠皮下移植实验证明FeⅢ-TA涂层在体内对ADSC spheroid生物活性无显著影响(P>0.05)。 (2)体外实验中,相较于native spheroid,spheroid@[FeⅢ-TA]3的三维球形状态维持时间更长(P<0.05),黏附相关基因的mRNA表达水平更低(P<0.05),抗炎因子白介素-1 受体拮抗剂(interleukin-1 receptor antagonist,IL-1RA)的 mRNA 表达和蛋白分泌更多(P<0.05),促进巨噬细胞向M2型巨噬细胞极化的作用更明显(P<0.05)。RNA测序实验结果显示spheroid@[FeⅢ-TA]3的三维状态和抗炎基因相关通路表达上调。 (3)体内实验中,照片观察、组织切片 HE染色和Masson染色结果显示,spheroid@[FeⅢ-TA]3处理组小鼠皮肤愈合效果优于普通细胞球处理组和空白对照组(P<0.05);组织切片 IL-1RA和CD206免疫荧光染色实验显示,相较于普通细胞球,spheroid@[FeⅢ-TA]3可以更好的促进IL-1 RA分泌和促进小鼠巨噬细胞向M2型巨噬细胞极化(P<0.05)。 结论: (1)FeⅢ-TA胶囊是一种生物相容性的材料,可以用来封装细胞微球。 (2)FeⅢ-TA胶囊可以延长ADSC spheroid的三维状态,同时增强其抗炎功能,从而促进小鼠皮肤伤口愈合。 ...
Copyright©2002-2026 Cnpowder.com.cn Corporation,All Rights Reserved